Nhuộm đặc biệt được sử sử dụng để đánh giá chất nhầy (bao gồm các phân tử và các đại phân tử chứa carbohydrate khác) và được sử dụng thường xuyên trong phòng thí nghiệm mô bệnh học. Bài viết này nhằm mục đích đánh giá cơ bản về cơ chế hoạt động của kỹ thuật nhuộm đặc biệt phổ biến bao gồm nhuộm xanh Alcian, nhuộm Mucicarmine, sắt Colloid và nhuộm Axit periodic – Schiff. Tuy nhiên, để hiểu được các cơ chế này, trước tiên cần xem xét cấu trúc cơ bản và tính chất hóa học của chất nhầy.
Giới thiệu về nhuộm đặc biệt
Chất nhầy là glycoprotein có trọng lượng phân tử cao, phân tán khắp biểu mô của đường tiêu hóa, hô hấp và sinh sản. Chất nhầy bao gồm một lõi protein ở trung tâm có gắn nhiều chuỗi carbohydrate (polysacarit). Hàm lượng carbohydrate trong phân tử chất nhầy có thể chiếm 60-80% trọng lượng phân tử. Lõi protein chứa hàm lượng cao các axit amin serine và threonine. Cấu trúc xác định của chất nhầy là sự hiện diện lặp lại song song của các chuỗi axit amin cụ thể trong lõi protein. Từ góc độ phân tử, chất nhầy được phân loại thành các họ riêng biệt (Muc 1, Muc 2, Muc 3, v.v.) dựa trên sự khác biệt về trình tự và kích thước của các lần lặp lại song song.
Có một số phân tử glycoprotein khác có cấu trúc tương tự với chất nhầy và thường bị nhầm lẫn với chất nhầy. Proteoglycan là phức hợp glycoconjugate có trọng lượng phân tử cao được tìm thấy ở nồng độ cao trong chất nền ngoại bào cũng như các mô liên kết. Proteoglycan thường được gọi là chất nhầy mô liên kết. Tuy nhiên, cấu trúc, (đặc biệt là lõi protein của proteoglycan), khác biệt với cấu trúc của chất nhầy.
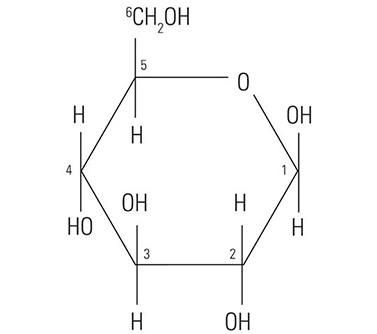
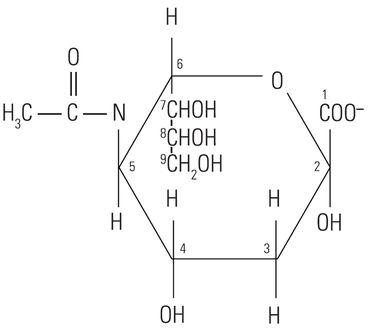
Lõi protein của chất nhầy ít hoặc không ảnh hưởng đến khả năng phản ứng mô hóa học của chất nhầy với thuốc nhuộm được sử dụng trong kỹ thuật nhuộm màu đặc biệt. Trên thực tế, khả năng phản ứng mô hóa phụ thuộc phần lớn vào thành phần carbohydrate của chất nhầy. “Carbohydrate” để mô tả một họ phân tử đa dạng có công thức chung Cn(H20)n. “Carbohydrate” thực chất là mô tả tỷ lệ 1:1 của phân tử carbon với nước (hydrat). Phân tử glucose (Hình 1) thể hiện cấu trúc của monosacarit carbohydrate điển hình. Các monosacarit tương tự khác là mannose và galactose. Những phân tử này không tích điện vì chúng không có nhóm ion hóa nào trong điều kiện bình thường. Ngược lại, các monosacarit khác có thể chứa các nhóm axit như nhóm carboxyl (COOH) và sulphonic (SO3H) có khả năng ion hóa để tạo ra điện tích âm tổng thể cho phân tử. Axit N-acetylneuraminic monosacarit carboxyl hóa thường được gọi là axit sialic được thể hiện trong (Hình 2). Sự hiện diện của các loại nhóm chức này xác định một phần khả năng phản ứng tiềm tàng với các thuốc nhuộm mô hóa học.
Từ góc độ mô hóa học, chất nhầy có thể được xếp vào một trong hai danh mục dựa trên tính chất hóa học và thành phần carbohydrate của chất nhầy. Chất nhầy tích điện hoặc “axit” chứa carbohydrate với nhóm carboxylate (COO–) hoặc sulphonate (SO3). Cả hai nhóm này đều bị ion hóa ở độ pH sinh lý để tạo ra điện tích âm tổng thể trên các phân tử chất nhầy này. Chuỗi carbohydrate của chất nhầy trung tính thiếu nhóm axit và do đó không mang điện tích. Các chất nhầy trung tính có thể được tìm thấy chủ yếu ở biểu mô bề mặt của dạ dày, tuyến Brunner của tá tràng và trong biểu mô tuyến tiền liệt. Chất nhầy axit được tìm thấy phân bố rộng khắp đường tiêu hóa và đường hô hấp.
Nhuộm đặc biệt ở chất nhầy sẽ chứa các phân tử thuốc nhuộm cation (tích điện dương) trong dung dịch ở độ pH cụ thể. Điều này đúng trong trường hợp của mucicarmine, nhuộm xanh Alcian cũng như các kỹ thuật nhuộm màu cũ hơn (sử dụng thuốc nhuộm xanh azure A hoặc xanh toluidine). Các phân tử thuốc nhuộm cation liên kết thông qua lực tĩnh điện với chuỗi polysacarit carboxyl hóa hoặc sunfat hóa anion của các phân tử chất nhầy.
Chất nhầy (Mucins)
Mucicarmine là một trong những kỹ thuật lâu đời nhất để xác định chất nhầy. Mặc dù không được sử dụng phổ biến như trước đây nhưng mucicarmine vẫn là một kỹ thuật có giá trị để đánh giá các chất nhầy axit, đặc biệt là các chất nhầy của đường tiêu hóa. Ngoài ra, kỹ thuật này còn hữu ích trong việc nhuộm vỏ nang của nấm Cryptococcus neoformans.
Phân tử thuốc nhuộm hoạt tính được tìm thấy trong mucicarmine là một phức hợp chelate được hình thành giữa các ion nhôm cation và axit carminic. Axit carminic là một phân tử thuốc nhuộm tự nhiên được phân lập từ cơ thể khô của côn trùng Coccus cacti cái. Các cation nhôm mang lại điện tích dương tổng thể cho phức hợp carmine. Mặc dù các cơ chế chính xác mà phức hợp này nhuộm có chọn lọc các chất nhầy vẫn chưa xác định, nhưng có thể cho thấy rằng đó là do lực hút tĩnh điện đối với các nhóm anion của chất nhầy axit. Định nghĩa này là từ các quan sát cho thấy rằng các vị trí mô chứa nhiều chất nhầy trung tính có ít hoặc không bị nhuộm màu trong khi các vị trí của đường tiêu hóa được biết là có chứa chất nhầy axit thường được nhuộm bằng mucicarmine.
Nhuộm xanh Alcian
Nhuộm xanh Alcian là một phân tử phthalocyanine cấu trúc phẳng với một nguyên tử đồng ở trung tâm. Phân tử này cũng chứa bốn nhóm isothiouronium cơ bản mang điện tích dương. Điện tích dương được truyền bởi các nhóm này dẫn đến sự thu hút các phân tử thuốc nhuộm xanh Alcian đến các vị trí anion trong phân tử chất nhầy. Giống như mucicarmine, màu xanh Alcian không làm ố các chất nhầy trung tính.
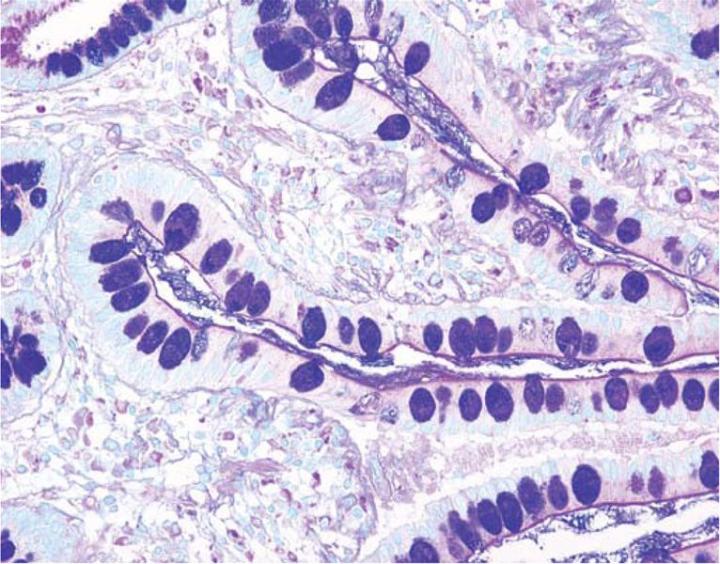
Thay đổi độ pH của thuốc nhuộm xanh Alcian là một phương tiện hữu ích để xác định thêm đặc tính của các phân nhóm chất nhầy axit có trong mẫu mô. Tất cả các chất nhầy có tính axit dù được carboxyl hóa hay sunfat hóa sẽ ion hóa ở độ pH 2,5 để tạo ra các nhóm anion (COO, SO3). Do đó, màu xanh Alcian tiêu chuẩn – pH 2,5 nhuộm tất cả các chất nhầy có tính axit (Hình 3). Ngược lại, chất nhầy có chứa chủ yếu là carbohydrate carboxyl hóa sẽ nhuộm xanh Alcian – pH 2.5 nhưng không có màu xanh Alcian ở pH 1.0. Các nhóm cacboxyl không bị ion hóa ở độ pH thấp hơn này và kết quả là chất nhầy sẽ có đặc tính trung tính. Các nhóm sulphonic có tính axit cao hơn có khả năng ion hóa ở độ pH=1, thích hợp để tiến hành nhuộm màu.
Nhuộm sắt Colloid
Kỹ thuật nhuộm sắt Colloid dựa trên sự hút các ion sắt tích điện dương (cation sắt) đối với các đầu nhóm carboxylate và sunfat tích điện âm trong chất nhầy có tính axit. Các ion sắt liên kết sẽ được xác định khi xử lý với kali ferrocyanide để tạo thành các cặn màu xanh sáng của ferrocyanide sắt hoặc xanh Phổ. Mặc dù kỹ thuật nhuộm sắt Colloid là một phương pháp cực kỳ nhạy để xác định chất nhầy axit nhưng nó không được sử dụng thường xuyên như nhuộm xanh Alcian. Tuy nhiên, giống như nhuộm xanh Alcian, kỹ thuật nhuộm sắt Colloid có thể được sử dụng kết hợp với axit periodic còn được gọi là kỹ thuật Schiff.
Nhuộm Axit periodic – Schiff (PAS)
Kỹ thuật PAS là kỹ thuật linh hoạt và được sử dụng rộng rãi nhất để biểu hiện glycoprotein, carbohydrate và chất nhầy. Không giống như các kỹ thuật khác đã mô tả, kỹ thuật PAS cũng sử dụng để nhận biết các chất nhầy trung tính. Khả năng phản ứng của kỹ thuật PAS không dựa trên sự hiện diện của các nhóm axit giữa các polysacarit mà thay vào đó dựa trên cấu trúc của các đơn vị monosacarit.
Kỹ thuật PAS dựa trên khả năng phản ứng của các nhóm aldehyd tự do trong các đơn vị monosacarit với thuốc thử Schiff để tạo thành sản phẩm cuối cùng có màu đỏ. Phản ứng ban đầu trong kỹ thuật PAS là quá trình oxy hóa các nhóm hydroxyl (OH) gắn với các nguyên tử cacbon liền kề. Các nhóm này được đề cập như là glycol 1, 2. Quá trình oxy hóa các glycol này dẫn đến sự hình thành các nhóm aldehyd phản ứng Schiff. Trong hầu hết các quy trình, dung dịch axit tuần hoàn 0,5% đến 1,0% được sử dụng làm chất oxy hóa.
Cường độ nhuộm màu sau phản ứng với thuốc thử Schiff tỷ lệ thuận với nồng độ của 1-2 nhóm glycol phản ứng trong mô. Kỹ thuật PAS cũng là phương pháp có độ nhạy cao trong việc xác định chất nhầy trung tính cũng như chất nhầy axit có chứa một lượng đáng kể axit sialic. Ngoài chất nhầy, kỹ thuật PAS cũng được sử dụng rộng rãi để phát hiện glycogen và các loại glycoprotein khác nhau. Kỹ thuật PAS đặc biệt có giá trị trong việc quan sát màng đáy dựa trên sự xuất hiện của phản ứng Schiff để xác định glycoprotein trong các cấu trúc này.
Nhuộm xanh Alcian / PAS
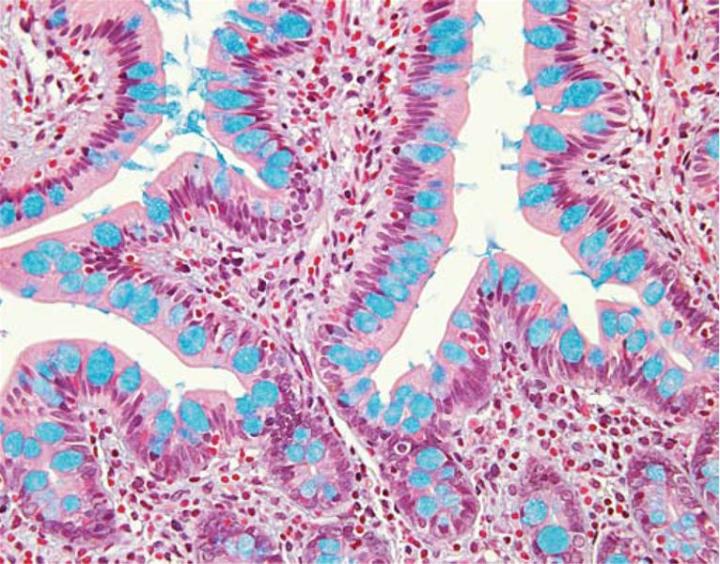
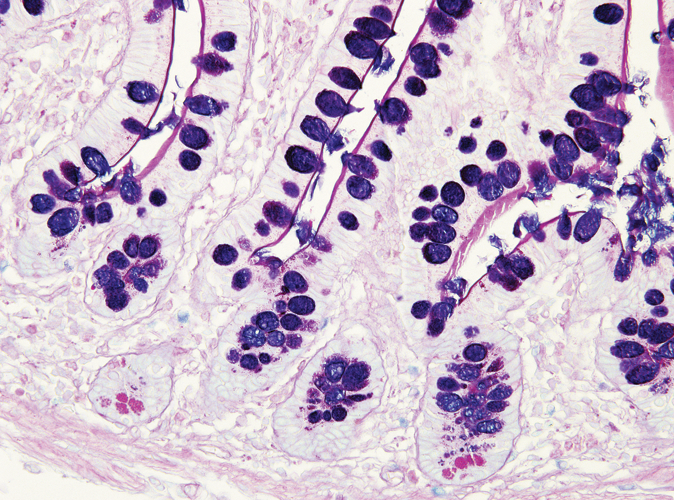
Sự kết hợp giữa kỹ thuật nhuộm xanh Alcian và PAS có thể được sử dụng như một phương pháp để phân biệt chất nhầy trung tính với chất nhầy axit. Trong hầu hết các quy trình, các phần được nhuộm bằng phương pháp nhuộm xanh Alcian tiêu chuẩn (pH 2,5), sau đó là kỹ thuật PAS. Nhuộm xanh Alcian ở độ pH 2,5 sẽ nhuộm tất cả các chất nhầy axit có màu xanh đậm nhưng sẽ không tạo màu cho các chất nhầy trung tính. Việc áp dụng kỹ thuật PAS tiếp theo sẽ làm cho chất nhầy trung tính có màu đỏ. Các mô hoặc tế bào chứa cả chất nhầy trung tính và axit có thể có màu xanh đậm hoặc tím (Hình 4). Kết hợp nhuộm xanh Alcian và PAS rất hữu ích vì một số lý do. Những thay đổi trong sự phân bố hoặc kiểu biểu hiện của chất nhầy trung tính và axit là dấu hiệu của một số tình trạng bệnh lý. Ngoài ra, kết hợp kỹ thuật nhuộm xanh Alcian /PAS sẽ là phương pháp có độ nhạy cao và toàn diện nhất để kiểm tra chất nhầy và tất cả chất nhầy sẽ phản ứng với bất kể tính chất điện tích.
Hình minh họa
Nguồn:
Minh Khang là nhà nhập khẩu và phân phối trực tiếp các sản phẩm nhuộm đặc biệt hãng


 EN
EN