Giới thiệu
Nhụy hoa nghệ tây (Saffron) được xem là loại gia vị đắt nhất thế giới. Hoa nghệ tây có màu tím và nhụy hoa màu đỏ dạng sợi được sử dụng làm gia vị và thuốc nhuộm tự nhiên. Vào mùa thu, các nhụy được hái thủ công và tách ra để tạo ra loại gia vị màu đỏ đặc trưng. Phải mất hơn 70.000 bông hoa để tạo ra chỉ một pound (0,45 kg) saffron. Màu vàng tự nhiên của nó đặc biệt hiệu quả khi dùng trong các món ăn như cơm saffron.
Crocins, dẫn xuất glycoside của crocetin và picrocrocin là những hợp chất tạo nên màu sắc và mùi vị của nghệ tây. Safranal, một aldehyd monoterpene, cũng như vậy. Ngoài ra, trong nghệ tây còn có các hợp chất có hoạt tính dược lý được công nhận, chẳng hạn như dẫn xuất crocin và flavonoid. Ví dụ, Saffron carotenoids đã được đề xuất như là chất chống ung thư, có thể điều trị một số bệnh ung thư một cách độc lập hoặc kết hợp với các hợp chất hóa học khác
Do đó, có rất nhiều tài liệu liên quan đến việc chiết xuất và phân tích nghệ tây. Thông thường, các thành phần được phân lập bằng sắc ký pha đảo (RPLC). Các dung môi điển hình là hỗn hợp nước/acetonitril hoặc nước/metanol. Như thường lệ, pha tĩnh là C18. Điều kiện tách ban đầu là hàm lượng nước cao, sử dụng gradient hàm lượng dung môi hữu cơ tăng lên đáng kể theo thời gian để rửa giải các hợp chất không phân cực. Axit formic thường được thêm vào pha động.
Sắc ký lỏng siêu tới hạn (SFC) là một loại sắc ký sử dụng carbon dioxide siêu tới hạn (CO2) làm một phần của pha động. Carbon dioxide siêu tới hạn có hệ số khuếch tán cao và độ nhớt thấp, khiến nó trở thành dung môi thích hợp để tách và phân tích các hợp chất. Sắc ký lỏng siêu tới hạn (SFC) cung cấp một số lợi thế so với các loại sắc ký khác, bao gồm thời gian phân tích nhanh hơn, sử dụng dung môi thấp hơn và độ chọn lọc khác nhau. Sắc ký lỏng siêu tới hạn (SFC) là một kỹ thuật trực giao so với RP-LC.
Bài viết này trình bày phương pháp tách chiết các thành phần chính của sợi nghệ tây sử dụng phương pháp phân tích sắc ký lỏng siêu tới hạn (SFC) với khối phổ (MS). Quá trình ion hóa chất phân tích được thực hiện bằng phương pháp ion hóa phun điện tử (ESI).
Vì pha động có tính axit nhẹ do sử dụng CO2 và metanol nên không cần sử dụng chất phụ gia.
Thiết bị
- Hệ thống sắc ký lỏng siêu tới hạn Sepiatec SFC
- Đầu dò CMS
- Nucleodur NH2 5 µm 250 x 4 mm
Hóa chất
- Carbon dioxide (99.9 %)
- Methanol (≥ 99 %)
- Sợi saffron
Thí nghiệm tách chiết sợi saffron từ nhụy hoa nghệ tây
Chuẩn bị mẫu:
1000 mg sợi saffron được chiết tách 5 lần với 10 mL metanol nóng. Dung dịch cuối cùng được lọc và sử dụng để phân lập hợp chất tự nhiên.
Điều kiện chạy:
Pha động: A = cacbon dioxit; B = metanol
Điều kiện pha động: 0 – 1 phút: 14 % B
1 – 18 phút: 14 – 18% B
18 – 40 phút: 18 – 50% B
40 – 44 phút: 50%B
Phát hiện: UV 440 nm
MS ESI (+/-)
Nucleodur NH2 5 µm 250 x 4 mm được điều hòa trong 5 phút ở tốc độ dòng 7 mL/phút với 86/14 % carbon dioxide siêu tới hạn và metanol. Các mẫu được tiêm tự động (V = 100 uL) bằng vòng mẫu và quá trình chạy đã bắt đầu (thời gian chạy = 44 phút). Bộ điều chỉnh áp suất ngược được đặt ở 150 bar và lò cột được làm nóng đến 40°C.
Kết quả
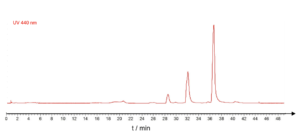
Việc chiết xuất các thành phần chính của Sợi saffron được thực hiện bằng metanol. Vì metanol là dung môi phân cực nên các hợp chất phân cực đặc biệt bị hòa tan. Hình 1 thể hiện sắc ký đồ UV ở bước sóng 440 nm. Trong 18 phút đầu tiên, không có hợp chất hoạt tính UV nào được rửa giải do đặc tính không phân cực của pha động (86 – 82 % CO2). Khi độ phân cực của pha động tăng dần theo gradient, một số hợp chất phân cực sẽ được rửa giải. Do việc phát hiện tia cực tím không cho phép nhận dạng các thành phần nên SFC được kết hợp với MS, cho phép nhận dạng liên tiếp. Hình 2 thể hiện sắc ký đồ UV và MS. Tín hiệu MS dựa trên các khối lượng khác nhau: (b) khối lượng 999 – 999,5 (ESI+); (c) khối lượng 836,9 – 837,4 (ESI+); (d) khối lượng 674,8 – 675,3 (ESI+); (e) khối lượng 975,5 – 976 (ESI-); (f) khối lượng 813,4 – 813,9 (ESI-); (g) khối lượng 651,4 – 651,9 (ESI-) và (h) khối lượng 341,2 – 341,7 (ESI-)
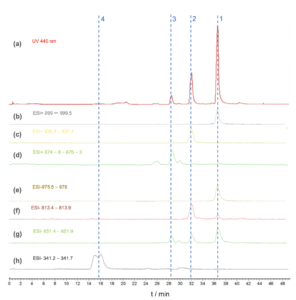
Bảng 1 cho thấy các hợp chất chính được MS xác định trong Hình 2. Các phân tử được ion hóa bằng ESI trong phân tích MS, đây là phương pháp ion hóa nhẹ ở áp suất khí quyển. Quá trình ion hóa có thể được thực hiện với điện áp dương (ESI+) hoặc điện áp âm (ESI-). Ở chế độ ion dương, các chất cộng natri ([M+Na]+) hoặc chất cộng proton ([M+H]+) thường được hình thành. Ở chế độ ion âm, ion ([M-H]-) thường được hình thành do mất đi một proton. Tùy thuộc vào mẫu và đặc tính của nó, nhiều sản phẩm tích điện cũng có thể được hình thành.
Crocetin xảy ra khi kết hợp với một số loại đường (glucose, gentibiose, triglucose và neapolitanoside) và do đó tạo thành crocin. Liên kết cộng hóa trị của crocetin với các phân tử đường dẫn đến sự gia tăng mạnh về độ phân cực và cung cấp cho crocins đặc tính ưa nước, đó là lý do tại sao các thành phần chính được xác định trong chất rửa giải AN này muộn. Trong bảng 1, có thể thấy rằng crocetin xuất hiện trong sợi saffron kết hợp với gentibiose và glucose.
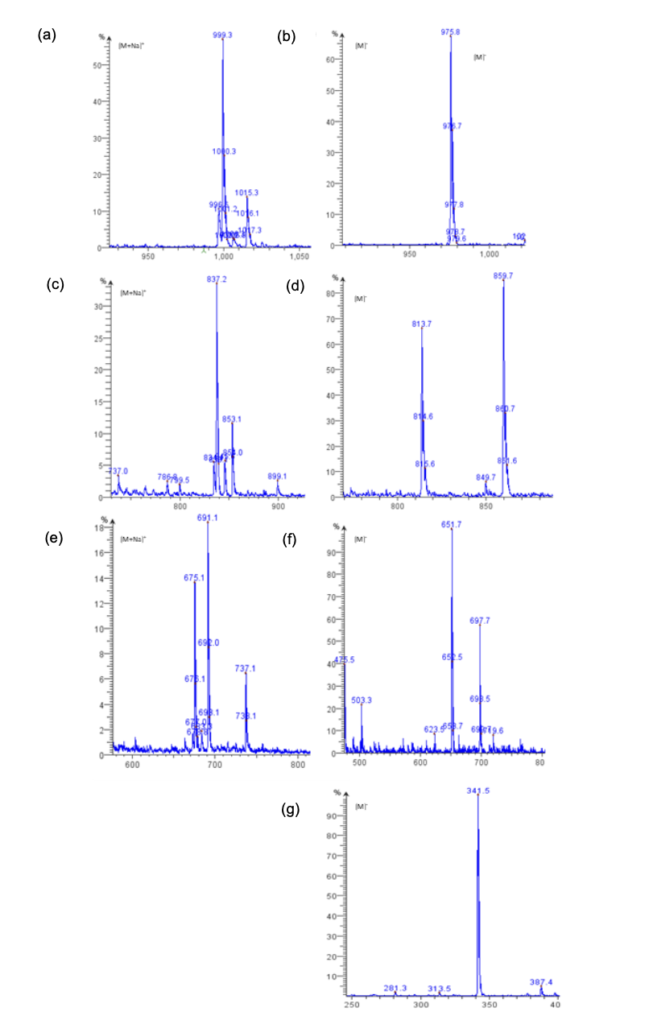
Hợp chất crocetin digentiobose ester bao gồm crocetin và hai phân tử gentiobose, được tạo thành từ 2 phân tử D-glucose. Trong Hình 2 (b), hợp chất được xác định có khối lượng 999 – 999,5 ở mức ion hóa dương. Chất cộng bao gồm natri (khối lượng 23 g/mol) và phân tử mẫu (khối lượng 976,4 g/mol). Phổ MS tương ứng được thể hiện trong Hình 3 (a). Este Crocetin digentiobose cũng có thể được phát hiện ở điện áp ion hóa âm (Hình 2 (e) khối lượng 975,5 – 976) Phổ MS tương ứng được thể hiện trong Hình 3 (b).
Crocetin gentiobiosyl glycosyl ester có thể được xác định ở cả chế độ ESI+ (Hình 2 (c)) và chế độ ESI- (Hình 2(f)) là ([M+Na]+ khối lượng 836,9 – 837,4) và ([M-H]- khối lượng 813,4 – 813.9), tương ứng. Phổ MS tương ứng được thể hiện trong Hình 3 (c) và (d). Hợp chất crocetin-gentiobiosyl glycosyl ester bao gồm các phân tử crocetin, gentiobose và D-glucose.
Crocetin gentiobiosyl ester có thể được xác định ở cả chế độ ESI+ (Hình 2 (d)) và chế độ ESI- (Hình 2(g)) là ([M + Na]+ khối lượng 674,8 – 675,3) và ([M – H]- khối lượng 651,4 – 651.9), tương ứng. Phổ MS tương ứng được thể hiện trong Hình 3 (e) và (f). Crocetin methyl ester chỉ có thể được xác định ở chế độ ESI- (Hình 2(h) khối lượng 341.2 – 341.7 và Hình 3(g)).
Trong ESI, các phân tử mẫu cũng bị phân mảnh, đó là lý do tại sao trong Hình 2, một số crocin được gán cho nhiều khối. Ví dụ, este crocetin digentiobose có thể bị ion hóa thành chất cộng ([M + Na]+) hoặc ([M – H]-), nhưng cũng có thể bị phân mảnh hơn nữa. Việc loại bỏ các nhóm glucose trong quá trình ion hóa âm sẽ tạo ra các mảnh có khối lượng tương tự như crocetin gentiobiosyl glycosyl ester và crocetin gentiobiosyl ester.
Bảng 1: Cấu trúc và trọng lượng phân tử của các thành phần chính của sợi saffron được xác định bởi MS (Hình 2).
| STT | Tên | Cấu trúc | Trọng lượng phân tử (g/mol) |
| 1 | Crocetin digentiobose ester |  |
976.4 C44H64O24 |
| 2 | Crocetin gentiobiosyl glycosyl ester |  |
814.8 C38H54O19 |
| 3 | Crocetingentiobiosyl ester |  |
652.7 C32H44O14 |
| 4 | Crocetin methyl ester | 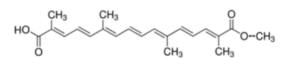 |
342.4 C21H26O4 |
Đối với hợp chất số 1, quá trình phân đoạn theo khối lượng được tiến hành ở cả hai chế độ ESI+ và ESI-, trong khi đối với hợp chất số 2, việc phân đoạn này chỉ được thực hiện ở chế độ ESI+. Hợp chất số 4 chỉ có thể được thu thập ở chế độ ESI. Tuy nhiên, sắc ký đồ khối lượng chiết được cho hợp chất số 3 rất phức tạp do có sự hiện diện của các mảnh có cấu trúc tương tự từ hợp chất số 1 và số 2, điều này đã cản trở quá trình phân đoạn theo hướng khối lượng. Thêm thời gian thực hiện để có thể giải quyết vấn đề này.
Kết luận
Các sản phẩm chưa được xác định thường bị hòa tan trong quá trình chiết tách khi phân tích sản xuất tự nhiên. Để xác định các thành phần này, cần thực hiện phương pháp MS. Trong nghiên cứu này, các thành phần chính của sợi saffron được chiết xuất bằng metanol và được phân tích bằng SFC-UV/MS. Việc xác định liên tiếp các thành phần chính được thực hiện bằng MS.
Nguồn:
Minh Khang là nhà phân phối và nhập khẩu trực tiếp các thiết bị sắc ký lỏng siêu tới hạn (SFC) hãng BUCHI.



 EN
EN